ползунки детские серый зверьки рост 74 см
ALLURE Колготки детские "Полоска" 50 ден серый

ALLURE Колготки детские "Полоска" 50 ден серый
230 Руб.WOOL&COTTON Носки детские Серый снеговик Merino

WOOL&COTTON Носки детские Серый снеговик Merino Носки и следки
600 Руб.WOOL&COTTON Носки детские Серый рубчик Merino

WOOL&COTTON Носки детские Серый рубчик Merino Носки и следки
600 Руб.Колготки детские для мальчика, Conte-kids, Tip-top 4С-03СП, темно-серые, 128-134 см, 476/6
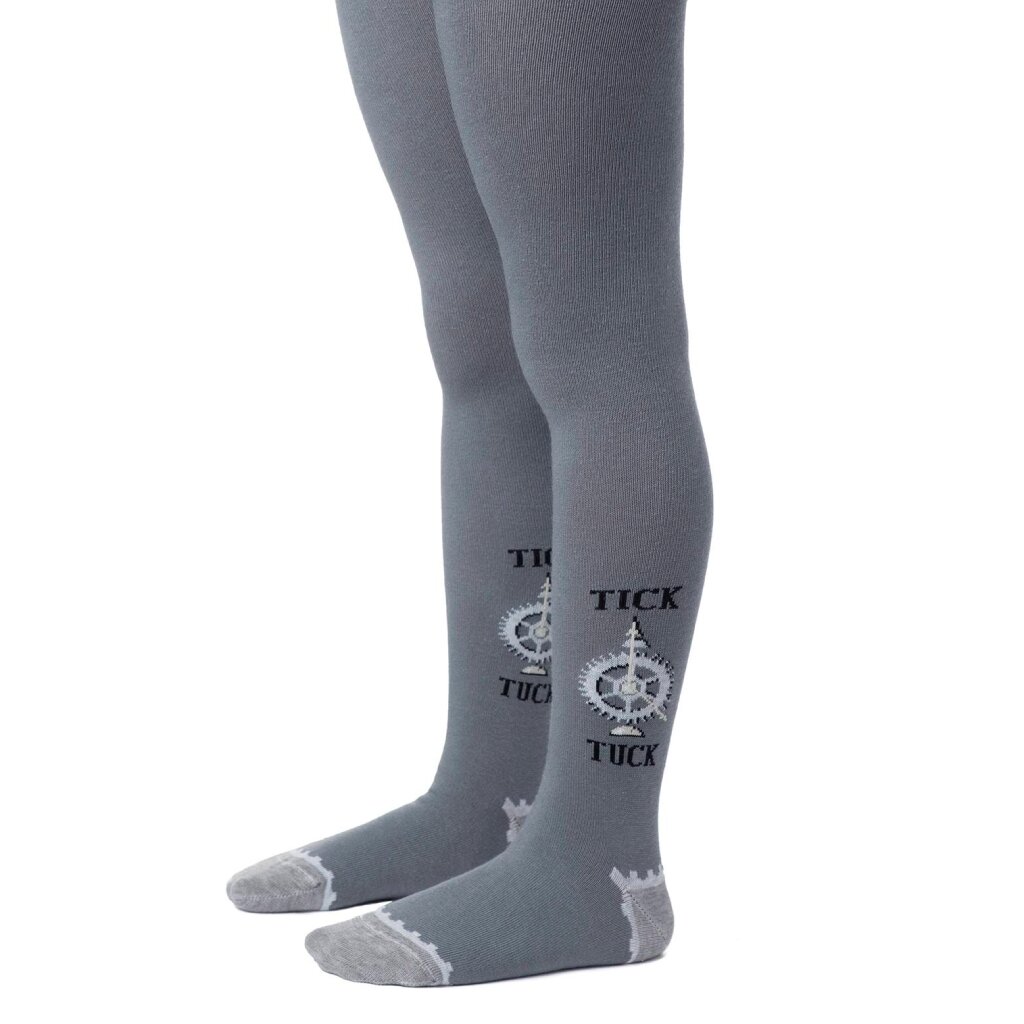
Детские колготки - это необходимый элемент гардероба для детей в холодное время года, который обеспечивает тепло и комфорт ногам ребенка, а также дополняет любой образ
382 Руб.Колготки детские для девочки, Conte-kids, Tip-top 14С-79 СП, светло-серые, 116-122 см, 510

Детские колготки - это необходимый элемент гардероба для детей в холодное время года, который обеспечивает тепло и комфорт ногам ребенка, а также дополняет любой образ
382 Руб.Колготки детские унисекс, Conte-kids, Tip-Top, серые, 140-146 см, 000

Детские колготки - это необходимый элемент гардероба для детей в холодное время года, который обеспечивает тепло и комфорт ногам ребенка, а также дополняет любой образ
415 Руб.Колготки детские унисекс, Conte-kids, Tip-Top, серые, 128-134 см, 000

Детские колготки - это необходимый элемент гардероба для детей в холодное время года, который обеспечивает тепло и комфорт ногам ребенка, а также дополняет любой образ
382 Руб.Колготки детские для девочки, Conte-kids, Tip-Top, 442, светло-серые, 150-152 см, 5С-07 СП

Детские колготки - это не просто предмет одежды, это способ выразить индивидуальность ребенка, подчеркнуть его стиль и настроение
413 Руб.Колготки детские Conte-kids, Class, 300, серые, р. 22, 150-152 см, 7С-31СП

Детские колготки - это не просто предмет одежды, это способ выразить индивидуальность ребенка, подчеркнуть его стиль и настроение
399 Руб.Колготки детские для девочки, Esli, 000, серые, р. 22, 150-152 см, 19С-188СПЕ

Детские колготки - это не просто предмет одежды, это способ выразить индивидуальность ребенка, подчеркнуть его стиль и настроение
375 Руб.Колготки детские для девочки, Esli, 000, серые, р. 23, 152-158 см, 19С-188СПЕ

Детские колготки - это не просто предмет одежды, это способ выразить индивидуальность ребенка, подчеркнуть его стиль и настроение
434 Руб.Колготки детские для девочки, Esli, 000, серые, р. 25, 158-164 см, 19С-188СПЕ

Детские колготки - это не просто предмет одежды, это способ выразить индивидуальность ребенка, подчеркнуть его стиль и настроение
415 Руб.Биогая Пробиотик капли Детские 5мл
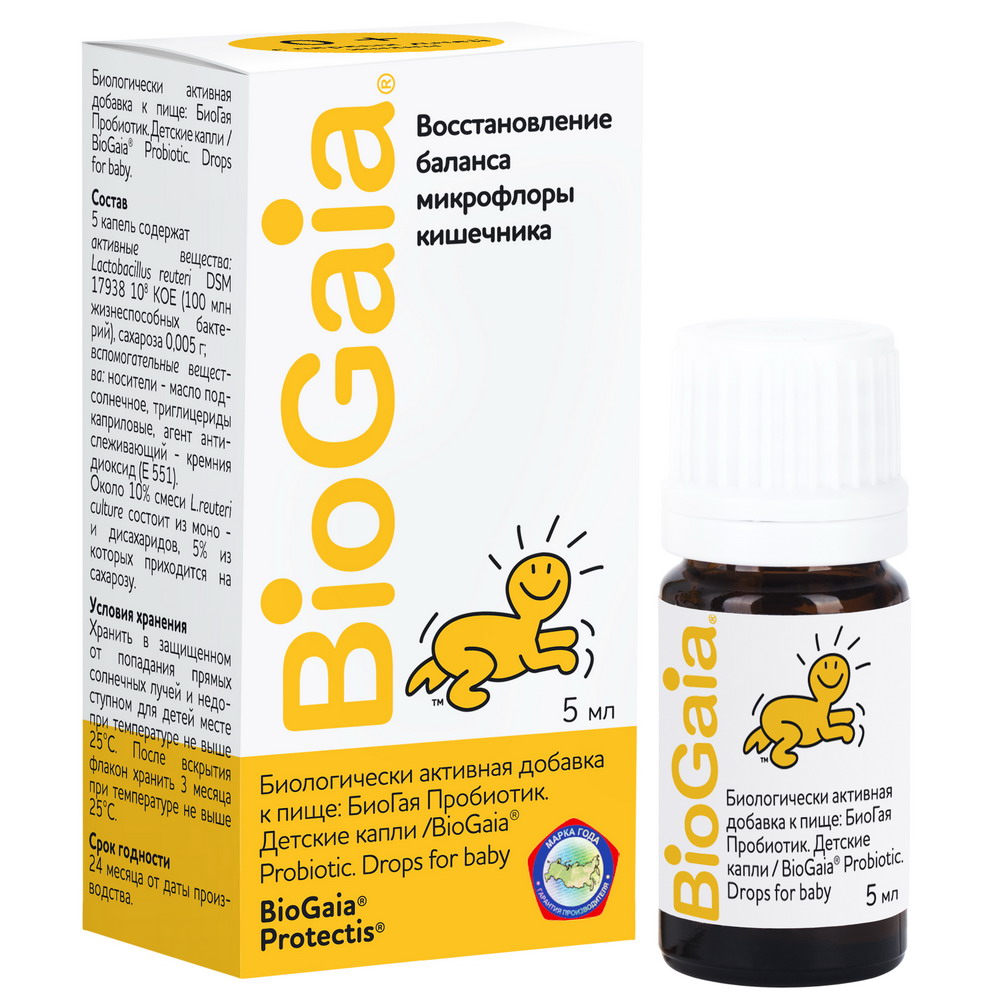
Состав Противопоказания Показания к применению Условия отпуска из аптек Условия хранения Способ применения и дозы Информация Состав Активное вещество: Lactobacillus reuteri Protectis (100 млн. КОЕ жизнеспособных бактерий в 5 каплях). Вспомогательные вещества: Подсолнечное масло, триглицериды каприловые, агент антислеживающий: кремния диоксид. Описание: Иммуностимулирующая активность L. reuteri Protectis связана с возможностью активизировать иммунную систему кишечника как первую линию защиты организма от инфекций за счет увеличения количества клеток CD4 + (специфическая подгруппа Т-лимфоцитов). Не содержит лактозу и белки молока. Форма выпуска: Капли с дисковым влагопоглотителем и дозатором во флаконе из темного стекла по 5 мл вместе с листком-вкладышем в картонной коробке. Противопоказания Повышенная чувствительность к составляющим компонентам. Не является лкарством. Показания к применению Рекомендуются в качестве дополнительного источника живых молочнокислых бактерий L. reuteri Protectis. reuteri Protectis - являются естественными микроорганизмами, которые впервые были выделены из грудного молока и в норме присутствуют в организме человека на всей протяженности желудочно-кишечного тракта. - колонизируют эпителий и размножаются во всех отделах ЖКТ, начиная с ротовой полости. - reuteri устойчивы к действию желудочного сока, солей желчных кислот и ферментов верхнего отдела тонкого кишечника. - поддерживают и регулируют физиологическое равновесие микрофлоры кишечника и активно участвуют в процессах пищеварения. - синтезируют молочную, уксусную кислоты и специфические вещества для этого вида лактобактерий - реутерин и рейтероциклин, подавляющие рост патогенных и условно-патогенных микроорганизмов в пищеварительном тракте. Усиливая естественную защиту пищеварительной системы от патогенных микроорганизмов, создают благоприятные условия для формирования нормального микробиоценоза кишечника. - способствует уменьшению интенсивности кишечных колик и длительности плача во время приступов кишечной колики у детей грудного возраста, а также частоты и продолжительности приступов. - обладают антагонистической активностью против H. pylori, а также уменьшают побочные реакции антибактериальной терапии при язвенной болезни желудка и двенадцатиперстной кишки. Условия отпуска из аптек Без рецепта. Условия хранения Хранить в упаковке производителя при температуре не выше 25 °С в сухом, защищенном от света и недоступном для детей месте. После вскрытия флакона хранить в течение 3 месяцев при температуре не выше 25 °С. Способ применения и дозы Для детей с первых дней жизни по 5 капель 1 раз в сутки. Для взрослых по 5 капель 1-2 раза в сутки. Длительность применения зависит от причины заболевания и индивидуальных особенностей организма. Перед началом применения рекомендована консультация врача. Био. Гая капли дают в ложке, можно добавлять к молоку, воде, другой жидкости или пище. Перед применением хорошо взболтать! Внимание! Для разведения капель использовать питьевую воду гарантированной безопасности и качества. Недопустимо использование питьевой воды из колодцев и каптажных источников. Не добавлять к горячему! Не изменяют вкус напитков и еды. Информация Внешний вид товара может отличаться от изображённого на фотографии. Имеются противопоказания. Необходимо ознакомиться с инструкцией или проконсультироваться со специалистом
0 Руб.Компливит Мама таб. п.о №100

Показания Профилактика и лечение гиповитаминоза и дефицита минеральных веществ: - в период подготовки к беременности (преконцепции): - во время беременности и грудного вскармливания. Противопоказания Противопоказания Повышенная чувствительность к компонентам препарата. Детский возраст. Гипервитаминоз А, повышенное содержание кальция и железа в организме, мочекаменная болезнь, пернициозная В 12-дефицитная анемия. С осторожностью: Беременность Нет данных Применение и дозы Перед применением необходимо проконсультироваться с врачом. Обычно рекомендуется принимать внутрь но 1 таблетке во время или сразу после завтрака, запивая обильным количеством жидкости. Длительность приема препарата определяется врачом. Побочные эффекты и передозировка Побочные эффекты: Возможны аллергические реакции. Передозировка: В случае передозировки необходимо обратиться к врачу. Лечение: временное прекращение приема препарата, промывание желудка, прием активированного угля внутрь, симптоматическое лечение. Взаимодействие с другими ЛС: Препарат содержит железо и кальций, поэтому задерживает всасывание в кишечнике антибиотиков из группы тетрациклинов и производных фторхинолона. При одновременном применении витамина С и сульфаниламидных препаратов короткого действия увеличивается риск развития кристаллурии. Антацидные препараты, содержащие алюминий, магний, кальций, а также колестирамин уменьшают всасывание железа. При одновременном назначении мочегонных средств из группы тиазидов увеличивается вероятность развития гиперкальциемии. Фармакологическое действие и фармакокинетика Комбинированный поливитаминный препарат с микро- и макроэлементами, совместимость компонентов в 1 таблетке обеспечена специальной технологией производства витаминно-минеральных комплексов. Действие препарата Компливит "МАМА" обусловлено эффектами входящих в его состав компонентов: а - Токоферола ацетат (витамин Е) - обладает антиоксидантными свойствами, поддерживает стабильность эритроцитов, предупреждает гемолиз: оказывает положительное влияние на функции половых желез, нервной и мышечной ткани. Дефицит витамина Е на ранних сроках беременности может явиться причиной выкидыша. Ретинола ацетат (витамин А) - играет важную роль в окислительно-восстановительных процессах, участвует в синтезе мукополисахаридов, белков, липидов. Способствует нормальному спермато- и овогенезу, развитию плаценты, росту, нормальному развитию и дифференцировки эмбриональных тканей, в т.ч. эпителиальных структур и костной ткани. Участвует в формировании зрительных пигментов, необходимых для нормального сумеречного и цветового зрения, обеспечивает целостность эпителиальных г камей. pei >- лируег рост костей. Тиамина гидрохлорид (витамин B1) - в качестве коэнзима участвуем в углеводном обмене, функционировании нервной системы. Рибофлавин (витамин В2) - важнейший катализатор процессов клеточного дыхания и зрительного восприятия. Пиридоксина гидрохлорид (витамин В6) - в качестве коэнзима принимает участие в белковом обмене и синтезе нейромедиаторов. Во время беременности необходим женщинам, ранее принимавшим пероральные контрацептивные средства, истощающие запасы пиридоксина в организме. Цианокобаламин (витамин В12) - участвует в синтезе нуклеотидов, является важным фактором нормального роста, кроветворения и развития эпителиальных клеток: необходим для метаболизма фолиевой кислоты и синтеза миелина. Никотинамид (витамин РР) участвует в процессах тканевого дыхания, жирового и углеводного обмена. Аскорбиновая кислота (витамин С) - обеспечивает синтез коллагена: участвует в формировании и поддержании структуры и функции хрящей, костей, зубов: влияет на образование гемоглобина, созревание эритроцитов. Витамин С повышает устойчивость организма к инфекциям, снижает воспалительные реакции. Кальция пантотенат - в качестве составной части коэнзима А играет важную роль в процессах ацетилирования и окисления: способствует построению, регенерации эпителия и эндотелия. Фолиевая кислота - принимает участие в синтезе аминокислот, нуклеотидов, нуклеиновых кислот: необходима для нормального эритропоэза. На ранних стадиях беременности снижает риск развития у плода дефектов нервной трубки, а также риск возникновения пороков челюстно-лицевой области. Железо - участвует в эритропоэзе, в составе гемоглобина обеспечивает транспорт кислорода в ткани: предупреждает развитие анемии у беременных женщин, особенно во II и III триместрах беременности. Медь - предупреждает анемию и кислородное голодание органов и тканей, способствует профилактики остеопороза. Укрепляет стенки сосудов. Марганец - предупреждает остеоартрит. Обладает противовоспалительными свойствами. Цинк - необходим для нормального формирования скелета плода и регенерации тканей, участвует в образовании некоторых гормонов, включая инсулин: снижает вероятность развития внутриутробных аномалий. В комплексе с витамином А способствует формированию нормального сумеречного и цветового зрения. Магний - нормализует артериальное давление, оказывает успокаивающее действие, уменьшает вероятность развития преэклампсии, самопроизвольного аборта, преждевременных родов. Кальций - необходим для формирования костного вещества, свертывания крови, осуществления процесса передачи нервных импульсов, сокращения скелетных и гладких мышц, нормальной деятельности миокарда. Фосфор - укрепляет костную ткань и зубы, усиливает минерализацию, входит в состав АТФ - источника энергии клеток. Фармакокинетика: Особые указания Не рекомендуется одновременное применение других поливитаминных комплексов во избежание передозировки. В период беременности суточная доза ретинола ацетата (в составе Компливита "МАМА") не должна превышать 5 тыс. ME. Возможно, окрашивание мочи в ярко-желтый свет, что совершенно безвредно и объясняется наличием в составе препарата рибофлавина. Влияние на способность управлять транспортными средствами: Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: Без рецепта Регистрационные данные Торговое название Компливит "Мама" для беременных и кормящих женщин Международное непатентованное название:Поливитамины + Минералы. Форма выпуска:таблетки покрытые пленочной оболочкой. Состав:Состав на одну таблетку Витамин А (ретинола ацетат) в виде порошка, содержащего ретинола ацетат, сахарозу, крахмал модифицированный, натрия-алюминия силикат, бутилгидрокситолуол, желатин, воду очищенную - 0,5675 мг (1650 ME) (в пересчете на 100% вещество). Витамин Е (а-токоферола ацетат) в виде порошка, содержащего DL-a-токоферола вещество) ацетат, желатин, сахарозу, кукурузный крахмал, натрия-алюминия силикат (Е 554), воду - 20,00 мг (в пересчете на 100 % вещество). Витамин В) (тиамина гидрохлорид) -2,00мг Витамин Вг (рибофлавин) - 2,00 мг Витамин Вб (пиридоксина гидрохлорид) - 5,00 мг Витамин С (аскорбиновая кислота) - 100,00 мг Никотинамид - 20,00 мг Фолиевая кислота - 0,40 мг Кальция пантотенат - 10,00 мг Витамин В12 (цианокобаламин)- 0,005 мг Эргокальциферол в виде маслянистой жидкости, содержащей Эргокальциферол и соевых бобов масло рафинированное, дезодорированное - 0,00625 мг (250 ME) (в пересчете на 100% вещество) Фосфор (в виде кальция гидрофосфата дигидрата) -19,00 мг Железо (в виде железа фумарата) - 10,00 мг Марганец (в виде марган ца сульфата моногидрата) - 2,50 мг Медь (в виде меди сульфата пентагидрата) - 2,00 мг Цинк (в виде цинка сульфата гептагидрата) - 10,00 мг Магний (в виде магния оксида) - 25,00 мг Кальций (в виде кальция гидрофосфата дигидрата) - 25,00 мг Вспомогательные вещества: кремния диоксид коллоидный (аэросил) - 6,72 мг, тальк - 5,01 мг, крахмал картофельный - 62,97 мг, лимонная кислота - 6,15 мг, повидон низкомолекулярный (поливинилпирролидон низкомолекулярный) - 6,04 мг, кальция стеарат - 8,20 мг, стеариновая кислота - 5,69 мг, сахароза (сахар) - 74,02 мг Состав оболочки: гипролоза - 7,6 мг, макрогол - 4000 - 3,18 мг, повидон низкомолекулярный (поливинилпирролидон низкомолекулярный) - 8,4 мг, титана диоксид - 5,73 мг, тальк - 5,4 мг, краситель азорубин (Е 122) - 0,04 мг, краситель тропеолин-0 - 0,15 мг. АТХ:A.11.A.A.04 Регистрация: Лекарственное средство Р N002958/01 Фармгруппа: поливитаминное средство+минералы. Дата регистрации: 13.10.2008. Окончание регстрации: . Описание:таблетки от желто-коричневого до светло-коричневого цвета с розоватым оттенком, двояковыпуклые продолговатой формы, покрытые пленочной оболочкой. Вид на изломе - желто-серый с вкраплениями разного цвета. Упаковка:Таблетки, покрытые оболочкой. По 30, 60 или 100 таблеток в банки полимерные. По 10 таблеток в контурную ячейковую упаковку. Каждую банку или 3, 6, 10 контурных ячейковых упаковок вместе с инструкцией по применению помещают в пачку из картона. Срок годности:2 года. Не использовать позже даты, указанной на упаковке. Владелец рег.удостоверения:ФАРМСТАНДАРТ-УфаВИТА, ОАО Производитель:ФАРМСТАНДАРТ-УфаВИТА, ОАО. Представительство:ФАРМСТАНДАРТ ОАО. Информация предоставлена: Компанией ГЭОТАР - http://www.lsgeotar.ru/
0 Руб.Тамифлю капс. 75мг №10
Показания Лечение гриппа у взрослых и детей в возрасте старше 1 года. Профилактика гриппа у взрослых и подростков в возрасте старше 12 лет, находящихся в группах повышенного риска инфицирования вирусом (в воинских частях и больших производственных коллективах, у ослабленных больных). Профилактика гриппа у детей старше 1 года. Противопоказания Противопоказания Повышенная чувствительность к осельтамивиру или любому компоненту препарата. Терминальная стадия почечной недостаточности (клиренс креатинина <:10 мл/мин). Детский возраст до 1 года. Тяжелая печеночная недостаточность. С осторожностью: Беременность, период грудного вскармливания. Беременность Контролируемых исследований у беременных женщин не проводилось. Однако результаты постмаркетинговых и наблюдательных исследований продемонстрировали пользу предлагаемого стандартного режима дозирования для данной популяции пациентов. Результаты фармакокинетического анализа показали более низкую экспозицию активного метаболита (приблизительно на 30% в течение всех триместров беременности) у беременных женщин по сравнению с не беременными. Тем не менее, значение расчетной экспозиции остается выше ингибирующих концентраций (значение IC95) и терапевтических значений для многих штаммов вируса гриппа. Изменение режима дозирования у беременных женщин при проведении терапии или профилактики не рекомендуется (см. раздел "Фармакокинетика в особых группах пациентов"). Не обнаружено прямого или опосредованного неблагоприятного влияния препарата на беременность, эмбрио-фетальное или постна- тальное развитие (см. "Доклинические данные"). При назначении Тамифлю® беременным женщинам следует учитывать как данные по безопасности, так и течение беременности и патогенность циркулирующего штамма вируса гриппа. Во время доклинических исследований осельтамивир и активный метаболит проникали в молоко лактирующих крыс. Данные по экскреции осельтамивира с грудным молоком у человека и применению осельтамивира кормящими женщинами ограничены. Осельтами- вир и его активный метаболит в небольших количествах проникают в грудное молоко (см. "Доклинические данные"), создавая субтерапевтические концентрации в крови грудного ребенка. При назначении осельтамивира кормящим женщинам следует также учитывать сопутствующее заболевание и патогенность циркулирующего штамма вируса гриппа. При беременности и в период [рудного вскармливания осельтамивир применяют только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода и ребенка. Применение и дозы Внутрь, во время еды или независимо от приема пищи. Переносимость препарата можно улучшить, если принимать его во время еды. Взрослые, подростки или дети, которые не могут проглотить капсулу, также могут получать лечение Тамифлю в лекарственной форме "порошок для приготовления суспензии для приема внутрь". В случаях, когда Тамифлю® в лекарственной форме "порошок для приготовления суспензии для приема внутрь" отсутствует, или при наличии признаков "старения" капсул (например, повышенная хрупкость или другие нарушения физического состояния), необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 чайная ложка) подходящего подслащенного продукта питания (шоколадный сироп с нормальным содержанием сахара или без содержания сахара, мед, светло-коричневый сахар или столовый сахар, растворенный в воде, сладкий десерт, сгущенное молоко с сахаром, яблочное пюре или йогурт) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же по- еле приготовления. Подробные рекомендации даны в подразделе "Экстемпоральное приготовление суспензии Тамифлю". Стандартный режим дозирования Лечение Прием препарата необходимо начинать не позднее 2 суток с момента развития симптомов заболевания. Взрослые и подростки в возрасте >:12 лет По 75 мг 2 раза в сутки внутрь в течение 5 дней. Увеличение дозы более 150 мг/сутки не приводит к усилению эффекта. Дети с массой тела >:40 кг или в возрасте от 8 до 12 лет Дети, которые умеют проглатывать капсулы, также могут получать лечение, принимая по одной капсуле 75 мг 2 раза в сутки в течение 5 дней. Дети в возрасте от 1 года до 8 лет Рекомендуется Тамифлю порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг (для детей старше 2 лет). Для определения рекомендованного режима дозирования смотрите инструкции по медицинскому применению Тамифлю порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг. Возможно экстемпоральное приготовление суспензии с использованием капсул 75 мг (см. подраздел "Экстемпоральное приготовление суспензии Тамифлю"). Профилактика Прием препарата необходимо начинать не позднее 2 суток после контакта с больными. Взрослые и подростки в возрасте >:12 лет По 75 мг 1 раз в сутки внутрь в течение не менее 10 дней после контакта с больным. Во время сезонной эпидемии гриппа - по 75 мг 1 раз в сутки в течение 6 недель. Профилактическое действие продолжается столько, сколько длится прием препарата. Дети с массой тела >:40 кг или в возрасте от 8 до 12 лет Дети, которые могут проглатывать капсулы, также могут получать профилактическую терапию, принимая по одной капсуле 75 мг 1 раз в сутки в течение 10 дней. Дети в возрасте от 1 года до 8 лет Рекомендуется Тамифлю порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг. Для определения рекомендованного режима дозирования смотрите инструкции по медицинскому применению Тамифлю® порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг. Возможно экстем- поральное приготовление суспензии с использованием капсул 75 мг (см. раздел "Экстемпоральное приготовление суспензии Тамифлю"). Дозирование в особых случаях Больные с поражением почек Лечение Больным с клиренсом креатинина более 60 мл/мин коррекции дозы не требуется. У боль- ных с клиренсом креатинина от 30 до 60 мл/мин дозу Тамифлю следует уменьшить до 30 мг два раза в сутки в течение 5 дней. У больных с клиренсом креатинина от 10 до 30 мл/мин дозу Тамифлю следует уменьшить до 30 мг один раз в сутки в течение 5 дней. Пациентам, находящимся на постоянном гемодиализе, Тамифлю в первоначальной дозе 30 мг можно принять до начала диализа, если симптомы гриппа появились в течение 48 ч между сеансами диализа. Для поддержания плазменной концентрации на терапевтическом уровне Тамифлю следует принимать по 30 мг после каждого сеанса диализа. Пациентам, находящимся на перитонеальном диализе, Тамифлю следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем но 30 мг каждые 5 дней (см. также "Дозирование в особых случаях" и "Особые указания"). Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина <:10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют. Профилактика Больным с клиренсом креатинина более 60 мл/мин коррекции дозы не требуется. У боль- ных с клиренсом креатинина от 30 до 60 мл/мин дозу Тамифлю следует уменьшить до 30 мг один раз в сутки. У больных с клиренсом креатинина от 10 до 30 мл/мин рекомендуется уменьшить дозу Тамифлю до 30 мг через день. Пациентам, находящимся на постоянном гемодиализе, Тамифлю в первоначальной дозе 30 мг можно принять до начала диализа ("1-й сеанс"). Для поддержания плазменной концентрации на терапевтическом уровне Тамифлю следует принимать по 30 мг после каждого последующего нечетного сеанса диализа. Пациентам, находящимся на перитонеальном диализе, Тамифлю следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем по 30 мг каждые 7 дней (см. также "Дозирование в особых случаях" и "Особые указания"). Фармакокинетика осельтами- вира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креа- тинина <:10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсу тствуют. Больные с поражением печени Коррекции дозы при лечении и профилактике гриппа у пациентов с нарушением функции печени легкой и средней степени тяжести не требуется. Безопасность и фармакокинетика Тамифлю у пациентов с тяжелыми нарушениями функции печени не изучалась. Больные пожилого и старческого возраста Коррекции дозы для профилактики или лечения гриппа не требуется. Вольные с ослабленным иммунитетом (после трансплантации) Для сезонной профилактики гриппа у больных с ослабленным иммунитетом в возрасте >:1 года - в течение 12 недель, коррекции дозы не требуется (см. раздел "Способ применения и дозы"). Дети Тамифлю® в данной лекарственной форме не следует назначать детям до 1 года. Экстемпоральное приготовление суспензии Тамифлю В случаях, когда у взрослых, подростков и детей существует проблема с проглатыванием капсул, а Тамифлю в лекарственной форме "порошок для приготовления суспензии для приема внутрь" отсутствует или при наличии признаков "старения" капсул, необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 чайная ложка) подходящего подслащенного продукта питания (см. выше) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же после приготовления. Если пациентам требуется доза 75 мг то необходимо следовать следующим инструкциям: 1. Держа одну капсулу 75 мг Тамифлю над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость. 2. Добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания (чтобы скрыть горький вкус) и хорошо перемешать. 3. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь. Если пациентам требуются дозы 30-60 мг, то для правильного дозирования необходимо следовать следующим инструкциям: 1. Держа одну капсулу 75 мг Тамифлю над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость. 2. Добавить в порошок 5 мл воды с помощью шприца с метками, показывающими количество набранной жидкости. Тщательно перемешать в течение 2 минут. 3. Набрать в ширин необходимое количество смеси из емкости согласно нижеприве ТАБЛИЦЪ Нет необходимости в заборе нерастворенного белого порошка, поскольку он является неактивным наполнителем. Нажав на поршень шприца, ввести все его содержимое во вторую емкость. Оставшуюся неиспользованную смесь необходимо выбросить. 4. Во вторую емкость добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания, чтобы скрыть горький вкус, и хорошо перемешать. 5. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь. Повторяйте данную процедуру перед каждым приемом препарата. Побочные эффекты и передозировка Побочные эффекты: В исследованиях по лечению гриппа у взрослых/пациентов подросткового возраста самыми частыми нежелательными реакциями (HP) были тошнота, рвота и головная боль. Большинство IIP возникали в первый или второй день лечения и проходили самостоятельно в течение 1-2 дней. В исследованиях по профилактике гриппа у взрослых и подростков самыми частыми НP были тошнота, рвота, головная боль и боль. У детей наиболее часто встречалась рвота. Описанные HP в большинстве случаев не требовали отмены препарата. Лечение и профилактика гриппа у взрослых и подростков В таблице 1 представлены НP, возникавшие наиболее часто (>:1%) при приеме рекомендованной дозы Тамифлю в исследованиях по профилактике и лечению гриппа у взрослых и подростков (75 мг 2 раза в сутки в течение 5 дней для лечения и 75 мг 1 раз в сутки до 6 недель для профилактики), и частота которых как минимум на 1% выше по сравнению с плацебо. В исследования по лечению гриппа вошли взрослые/подростки без сопутствующей патологии и больные группы риска, т.е. пациенты с высоким риском развития осложнений гриппа (пациенты пожилого и старческого возраста, пациенты с хроническими заболеваниями сердца или органов дыхания). В целом профиль безопасности у пациентов группы риска соответствовал таковому у взрослых/пациентов подросткового возраста без сопутствующей патологии. В исследованиях по профилактике гриппа профиль безопасности у пациентов, получав- ших рекомендованную дозу Тамифлю (75 мг 1 раз в сутки до 6 недель), не отличался от такового в исследованиях по лечению гриппа, несмотря на более длительный прием препарата. лечение - дерматит (включая аллергический и атопический дерматит, 1% против 2%). Нарушения со стороны органа слуха и лабиринтные нарушения (Тамифлю против плацебо): лечение - боль в ухе (1% против 1%). Нарушения со стороны органа зрения (Тамифлю против плацебо): лечение- конъюнктивит (включая покраснение глаз, выделения из глаза и боль в глазах, 1% против <:1%). Дополнительные нежелательные явления, отмеченные при проведении лечения гриппа у детей, не соответствовавшие описанным выше критериям. Нарушения со стороны крови и лимфатической системы (Тамифлю против плацебо): лечение - лимфоаденопатия (<:1% против 1%). Нарушения со стороны органа слуха и лабиринтные нарушения (Тамифлю против плацебо): лечение - повреждение барабанной перепонки (<:1% против 1%). Постмаркетинговое наблюдение Далее представлены нежелательные явления при применении Тамифлю, которые наблюдались в период постмаркетингового наблюдения. Частота данных нежелательных явлений и/или причинно-следственная связь с применением препарата Тамифлю® не может быть установлена, так как не известен истинный размер популяции в виду добровольного характера сообщений. Нарушения со стороны кожи и подкожных тканей: реакции гиперчувствительности - дерматит, кожная сыпь, экзема, крапивница, мультиформная экссудативная эритема, синдром Стивенса-Джонсона и токсический эпидермальный некролиз, аллергия, анафилактические и анафилактоидные реакции, отек Квинке. Нарушения со стороны печени и желчевыводящих путей: гепатит, увеличение активности "печеночных" ферментов у пациентов с гриппоподобными симптомами, получавших Тамифлю: фульминантный гепатит (в том числе с фатальным исходом), печеночная недостаточность, желтуха. Нарушения со стороны нервно-психической сферы Гриппозная инфекция может ассоциироваться с различными неврологическими симптомами и изменениями поведения, включая такие симптомы, как галлюцинации, бред и анормальное поведение. В некоторых случаях они могут привести к смертельному исходу. Такие явления могут возникать как на фоне развития энцефалопатии или энцефалита, так и без проявления данных заболеваний. У пациентов (в основном у детей и подростков), принимавших Тамифлю с целью лечения гриппа, были зарегистрированы судороги и делирий (включая такие симптомы, как нарушение сознания, дезориентация во времени и пространстве, анормальное поведение, бред, галлюцинации, возбуждение, тревога, ночные кошмары). Эти случаи редко сопро- вождались опасными для жизни действиями. Роль Тамифлю в развитии этих явлений неизвестна. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших Тамифлю. Нарушения со стороны желудочно-кишечного тракта: желудочно-кишечные кровотечения после приема Тамифлю® (в частности, нельзя исключить связь между явлениями геморрагического колита и приемом Тамифлю, поскольку указанные явления исчезали как после выздоровления пациента от гриппа, так и после отмены препарата). Нарушения со стороны органа зрения: нарушение зрения. Нарушения со стороны сердца: аритмия. Передозировка: В большинстве случаев передозировка в ходе клинических исследований и при постмар- кетинговом применении Тамифлю не сопровождалась какими-либо нежелательными явлениями. В остальных случаях симптомы передозировки соответствовали нежелательным явлениям, представленным в разделе "Побочное действие". Взаимодействие с другими ЛС: Клинически значимые лекарственные взаимодействия маловероятны по данным фармакологических и фармакокинетических исследований. Осельтамивир экстенсивно превращается в активный метаболит под действием эстераз, в основном расположенных в печени. Лекарственные взаимодействия, обусловленные конкуренцией за связывание с активными центрами эстераз, в литературных источниках широко не представлены. Низкая степень связывания осельтамивира и активного метаболита с белками плазмы не дают оснований предполагать наличие взаимодействий, связанных с вытеснением лекарственных средств из связи с белками. Исследования in vitro показывают, что ни осельтамивир, ни его активный метаболит не являются предпочтительным субстратом для полифункциональных оксидаз системы цитохрома Р450 или для глюкуронилтрансфераз (см. подраздел "Фармакокинетика"). Оснований для взаимодействия с пероральными контрацептивами нет. Циметидин, неспецифический ингибитор изоферментов системы цитохрома Р450 и конкурирующий в процессе канальцевой секреции с препаратами щелочного типа и катионами, не влияет на плазменные концентрации осельтамивира и его активного метаболита. Маловероятны клинически значимые межлекарственные взаимодействия, связанные с конкуренцией за канальцевую секрецию, принимая во внимание резерв безопасности для большинства подобных препаратов, пути выведения активного метаболита осельтамивира (клубочковая фильтрация и анионная канальцевая секреция), а также выводящую способность каждого из путей. Пробенецид приводит к увеличению AUC активного метаболита осельтамивира примерно в 2 раза (за счет снижения активной канальцевой секреции в почках). Однако коррекции дозы при одновременном применении с пробенецидом не требуется, учитывая резерв безопасности активного метаболита. Одновременный прием с амоксициллином не влияет на плазменные концентрации осель- тамивира и его компонентов, демонстрируя слабую конкуренцию за выведение путем анионной канальцевой секреции. Одновременный прием с парацетамолом не влияет на плазменные концентрации осельтамивира и его активного метаболита или парацетамола. Фармакокинетических взаимодействий между осельтамивиром, его основным метаболитом не обнаружено при одновременном приеме с парацетамолом, ацетилсалициловой кислотой, циметидином, антацидными средствами (магния и алюминия гидроксид, кальция карбонат), варфарином, римантадином или амантадином. При использовании Тамифлю с часто применяемыми препаратами, такими как ингибиторы АПФ (эналаприл, каптоприл), тиазидные диуретики (бендрофлуметиазид), антибиотики (пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин), блокато- ры Н2-гистаминовых рецепторов (ранитидин, циметидин), бета-адреноблокаторы (про- пранолол), ксантины (теофиллин), симпатомиметики (псевдоэфедрин), опиаты (кодеин), глюкокортикостероиды, ингаляционные бронхолитики и ненаркотические анальгетики (ацетилсалициловая кислота, ибупрофен и парацетамол), изменений характера или частоты нежелательных явлений не наблюдалось. Применять осельтамивир в комбинации с препаратами, имеющими узкую широту терапевтического действия (например, хлорпропамид, метотрексат, бутадион), необходимо с осторожностью. Фармакологическое действие и фармакокинетика Механизм действия Противовирусный препарат. Осельтамивир является пролекарством, его активный метаболит (осельтамивира карбоксилат, ОК) - эффективный и селективный ингибитор нейра- минидазы вирусов гриппа типа А и В - фермента, катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновения в неинфицированные клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме. Тормозит рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo, уменьшает выделение вирусов гриппа А и В из организма. Концентрация ОК, необходимая для ингибирования нейраминидазы на 50% (IC50), составляет 0.1-1.3 нМ для вируса гриппа А и 2.6 нМ для вируса гриппа В. Медиана значений IC50 для вируса гриппа В несколько выше и составляет 8.5 нМ. Клиническая эффективность В проведенных исследованиях Тамифлю не оказывал влияния на образование противогриппозных антител, в том числе на выработку антител в ответ на введение инактивированной вакцины против гриппа. Исследования естественной гриппозной инфекции В клинических исследованиях, проведенных во время сезонной инфекции гриппа, пациенты начинали получать Тамифлю® не позднее 40 ч после появления первых симптомов гриппозной инфекции. 97% пациентов были инфицированы вирусом гриппа А и 3% пациентов - вирусом гриппа В. Тамифлю значительно сокращал период клинических проявлений гриппозной инфекции (на 32 ч). У пациентов с подтвержденным диагнозом гриппа, принимавших Тамифлю, тяжесть заболевания, выраженная как площадь под кривой для суммарного индекса симптомов, была на 38% меньше по сравнению с пациентами, получавшими плацебо. Болес того, у молодых пациентов без сопутствующих заболеваний Та- мифлю снижал примерно на 50% частоту развития осложнений гриппа, требующих применения антибиотиков (бронхита, пневмонии, синусита, среднего отита). Были получены четкие доказательства эффективности препарата в отношении вторичных критериев эффективности, относящихся к антивирусной активности: Тамифлю вызывал как укорочение времени выделения вируса из организма, так и уменьшение площади под кривой "вирусные тигры-время". Данные, полученные в исследовании по терапии Тамифлю у больных пожилого и старческого возраста, показывают, что прием Тамифлю в дозе 75 мг 2 раза в сутки в течение 5 дней сопровождался клинически значимым уменьшением медианы периода клинических проявлений гриппозной инфекции, аналогичным таковому у взрослых пациентов более молодого возраста, однако различия не достигли статистической значимости. В другом исследовании больные гриппом старше 13 лет, имевшие сопутствующие хронические заболевания сердечно-сосудистой и/или дыхательной систем, получали Тамифлю в том же режиме дозирования или плацебо. Отличий в медиане периода до уменьшения клинических проявлений гриппозной инфекции в группах Тамифлю и плацебо не было, однако период повышения температуры при приеме Тамифлю сокращался примерно на 1 день. Доля пациентов, выделяющих вирус на 2-ой и 4-ый день, становилась значительно меньше. Профиль безопасности Тамифлю у пациентов группы риска не отличался от такового в общей популяции взрослых пациентов. Лечение гриппа у детей У детей в возрасте 1-12 лет (средний возраст 5.3 года), имевших лихорадку (>:37.8оС) и один из симптомов со стороны дыхательной системы (кашель или ринит) в период циркуляции вируса гриппа среди населения, было проведено двойное слепое плацебо- контролируемое исследование. 67% пациентов были инфицированы вирусом гриппа А и 33% пациентов - вирусом гриппа В. Препарат Тамифлю (при приеме не позднее 48 ч после появления первых симптомов гриппозной инфекции) значительно снижал продолжительность заболевания (на 35.8 ч) по сравнению с плацебо. Продолжительность заболевания определялась как время до купирования кашля, заложенности носа, исчезновения лихорадки, возвращения к обычной активности. В группе детей, получавших Тамифлю®, частота острого среднего отита снижалась на 40% по сравнению с группой плацебо. Выздоровление и возвращение к обычной активности наступало почти на 2 дня раньше у детей, получавших Тамифлю®, по сравнению с группой плацебо. В другом исследовании участвовали дети в возрасте 6-12 лет, страдающие бронхиальной астмой: 53.6% пациентов имели гриппозную инфекцию, подтвержденную серологически и/или в культуре. Медиана продолжительности заболевания в группе пациентов, полу- чавших Тамифлю , значительно не снижалась. Но к последнему 6-му дню терапии Тамифлю® объем форсированного выдоха за 1 сек (ОФВ1) повышался на 10.8% по сравнению с 4.7% у пациентов, получавших плацебо (р=0.0148). Профилактика гриппа у взрослых и подростков Профилактическая эффективность Тамифлю при естественной гриппозной инфекции А и В была доказана в 3 отдельных клинических исследованиях III фазы. На фоне приема Тамифлю® гриппом заболели около 1% пациентов. Тамифлю® также значительно уменьшал частоту выделения вируса и предотвращал передачу вируса от одного члена семьи к другому. Взрослые и подростки, которые были в контакте с больным членом семьи, начинали прием Тамифлю® в течение двух дней после возникновения симптомов гриппа у членов семьи и продолжали его в течение 7 дней, что достоверно уменьшало частоту случаев гриппа у контактировавших лиц на 92%. У непривитых и в целом здоровых взрослых в возрасте 18-65 лет прием Тамифлю во время эпидемии гриппа существенно снижал заболеваемость гриппом (на 76%). Пациенты принимали препарат в течение 42 дней. У лиц пожилого и старческого возраста, находившихся в домах для престарелых, 80% из которых были привиты перед сезоном, когда проводилось исследование, Тамифлю достоверно снижал заболеваемость гриппом на 92%. В том же исследовании Тамифлю достоверно (на 86%) уменьшал частоту осложнений гриппа: бронхита, пневмонии, синусита. Пациенты принимали препарат в течение 42 дней. Профилактика гриппа у детей Профилактическая эффективность Тамифлю при естественной гриппозной инфекции была продемонстрирована у детей от 1 года до 12 лет после контакта с заболевшим членом семьи или с кем-то из постоянного окружения. Основным параметром эффективности была частота лабораторно подтвержденной гриппозной инфекции. У детей, получавших Тамифлю /порошок для приготовления суспензии для приема внутрь/ в дозе от 30 до 75 мг 1 раз в день в течение 10 дней и не выделявших вирус исходно, частота лабораторно подтвержденного гриппа уменьшилась до 4% (2/47) по сравнению с 21% (15/70) в группе плацебо. Профилактика гриппа у лиц с ослабленным иммунитетом У лиц с ослабленным иммунитетом при сезонной гриппозной инфекции и при отсутствии вирусовыделения исходно, профилактическое применение Тамифлю приводило к снижению частоты лабораторно подтвержденной гриппозной инфекции, сопровождающейся клинической симптоматикой, до 0.4% (1/232) по сравнению с 3% (7/231) в группе плацебо. Лабораторно подтвержденная гриппозная инфекция, сопровождающаяся клинической симптоматикой, диагностировалась при наличии температуры в полости рта выше 37.2°С, кашля и/или острого ринита (все зарегистрированные в один и тот же день во время приема препарата/плацебо), а также положительного результата обратно-транскриптазной полимеразной цепной реакции на РНК вируса гриппа. Резистентность Клинические исследования Риск появления вирусов гриппа со сниженной чувствительностью или резистентностью к препарату изучался в клинических исследованиях, спонсированных компанией Рош. У всех пациентов-носителей OK-резистентного вируса носительство имело временный характер, не влияло па элиминацию вируса и не вызывало ухудшения клинического состояния. ТАБЛИЦЪ При приеме Тамифлю с целью постконтактной профилактики (7 дней), профилактики контактировавших в семье (10 дней) и сезонной профилактики (42 дня) у лиц с нормальной функцией иммунной системы случаев резистентности к препарату не отмечено. В 12-недельном исследовании по сезонной профилактике у лиц с ослабленным иммунитетом случаев возникновения резистентности также не наблюдалось. Данные отдельных клинических случаев и наблюдательных исследовании У пациентов, не получавших осельтамивир, обнаружены возникающие в природных условиях мутации вирусов гриппа А и В, которые обладали сниженной чувствительностью к осельтамивиру. В 2008 году мутация по типу замены H275Y. приводящая к резистентности, была обнаружена более чем у 99% штаммов вируса 2008 Н1N1, циркулирующих в Европе. Вирус гриппа 2009 H1N1 ("свиной грипп") в большинстве случаев был чувствителен к осельтамивиру. Устойчивые к осельтамивиру штаммы обнаружены у лиц с нормальной функцией иммунной системы и лиц с ослабленным иммунитетом, принимавших осельта- мивир. Степень снижения чувствительности к осельтамивиру и частота встречаемости подобных вирусов может отличаться в зависимости от сезона и региона. Устойчивость к осельтамивиру обнаружена у пациентов с пандемическим гриппом H1N1, получавших препарат как для лечения, так и для профилактики. Частота встречаемости резистентности может быть выше у более молодых пациентов и пациентов с ослабленным иммунитетом. Устойчивые к осельтамивиру лабораторные штаммы вирусов гриппа и вирусы гриппа от пациентов, получавших терапию осельтами- виром, несут мутации нейраминидазы N1 и N2. Мутации, приводящие к устойчивости, часто являются специфическими для подтипа нейраминидазы. При принятии решения о применении Тамифлю следует учитывать сезонную чувствительность вируса гриппа к препарату (последнюю информацию можно найти на сайте ВОЗ). Доклинические данные Доклинические данные, полученные на основании стандартных исследований по изучению фармакологической безопасности, генотоксичности и хронической токсичности, не выявили особой опасности для человека. Канцерогенность: результаты 3-х исследований по выявлению канцерогенного потенциала (двух 2-х летних исследований на крысах и мышах для осельтамивира и одного 6-ти месячного исследования на трансгенных мышах Tg:AC для активного метаболита) были отрицательными. Мутагенность: стандартные генотоксические тесты для осельтамивира и активного метаболита были отрицательными. Влияние на фертильность: осельтамивир в дозе 1500 мг/кг/сут не влиял на генеративную функцию самцов и самок крыс. Тератогенность: в исследованиях по изучению тератогенности осельтамивира в дозе до 1500 мг/кг/сут (на крысах) и до 500 мг/кг/сут (на кроликах) влияния на эмбрио-фетальное развитие не обнаружено. В исследованиях но изучению антенатального и постнатального периодов развития у крыс при введении осельтамивира в дозе 1500 мг/кг/сут наблюдалось увеличение периода родов: предел безопасности между экспозицией для человека и максимальной не оказывающей эффекта дозой у крыс (500 мг/кг/сут) для осельтамивира выше в 480 раз, а для его активного метаболита - в 44 раза. Экспозиция у плода составляла 15- 20% от таковой у матери. Прочее: осельтамивир и активный метаболит проникают в молоко лактирующих крыс. Согласно ограниченным данным осельтамивир и его активный метаболит проникают в грудное молоко человека. По результатам экстраполяции данных, полученных в исследованиях у животных, их количество в грудном молоке может составлять 0.01 мг/сутки и 0.3 м г/сутки, соответственно. Примерно у 50% протестированных морских свинок при введении максимальных доз активной субстанции осельтамивира наблюдалась сенсибилизация кожи в виде эритемы. Также выявлено обратимое раздражение глаз у кроликов. В то время как очень высокие пероральные однократные дозы (657 мг/кг и выше) осельтамивира не оказывали влияния на взрослых крыс, данные дозы оказывали токсическое действие на незрелых 7-дневных детенышей крыс, в том числе приводили к гибели животных. Нежелательных эффектов не наблюдалось при хроническом введении в дозе 500 мг/кг/сут с 7 по 21 день постнаталыюго периода. Фармакокинетика: Всасывание Осельтамивир легко всасывается в желудочно-кишечном тракте и экстенсивно превращается в активный метаболит под действием печеночных и кишечных эстераз. Концентрации активного метаболита в плазме определяются в пределах 30 мин, время достижения максимальной концентрации 2-3 ч, и более чем в 20 раз превышают концентрации пролекарства. Не менее 75% принятой внутрь дозы попадает в системный кровоток в виде активного метаболита, менее 5% - в виде исходного препарата. Плазменные концентрации как пролекарства, так и активного метаболита пропорциональны дозе и не зависят от приема пищи. Распределение Объем распределения (Vss) активного метаболита - 23 л. По данным исследований, проведенных на животных, после приема внутрь осельтамивира его активный метаболит обнаруживался во всех основных очагах инфекции (легких, промывных водах бронхов, слизистой оболочке полости носа, среднем ухе и трахее) в концентрациях, обеспечивающих противовирусный эффект. Связь активного метаболита с белками плазмы - 3%. Связь пролекарства с белками плазмы - 42%, что недостаточно, чтобы служить причиной существенных лекарственных взаимодействий. Метаболизм Осельтамивир экстенсивно превращается в активный метаболит под действием эстераз, находящихся преимущественно в печени. Ни осельтамивир, ни активный метаболит не являются субстратами или ингибиторами изоферментов системы цитохрома Р450. Выведение Выводится (>:90%) в виде активного метаболита преимущественно почками. Активный метаболит не подвергается дальнейшей трансформации и выводится почками (>:99%) путем клубочковой фильтрации и канальцевой секреции. Почечный клиренс (18.8 л/ч) превышает скорость клубочковой фильтрации (7.5 л/ч), что указывает на то, что препарат выводится еще и путем канальцевой секреции. Через кишечник выводится менее 20% принятого препарата. Период полувыведения активного метаболита 6-10 ч. Фармакокинетика в особых группах пациентов Больные с поражением почек При применении Тамифлю (100 мг два раза в сутки в течение 5 дней) у больных с различной степенью поражения почек площадь под кривой "концентрация активного метаболита в плазме - время" (AUC оселыамнвира карбоксилата) обратно пропорциональна снижению функции почек. Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина <:10 мл/мин), не находящихся на диализе, не изучалась. Больные с поражением печени Полученные in vitro и в исследованиях на животных данные об отсутствии значительного повышения AUC осельтамивира или его активного метаболита при нарушении функции печени легкой и средней степени тяжести были подтверждены и в клинических исследованиях (см. "Дозирование в особых случаях"). Безопасность и фармакокинетика оссльта- мивира у пациентов с тяжелым нарушением функции печени не изучалась. Вольные пожилого и старческого возраста У больных пожилого и старческого возраста (65-78 лет) экспозиция активного метаболита в равновесном состоянии на 25-35% выше, чем у более молодых пациентов при назначении аналогичных доз Тамифлю. Период полувыведения препарата у больных пожилого и старческого возраста существенно не отличался от такового у более молодых пациентов. С учетом данных по экспозиции препарата и его переносимости больными пожилого и старческого возраста коррекции дозы при лечении и профилактике гриппа не требуется. Лети в возрасте от 1 года до 8 лет и подростки Фармакокинетику Тамифлю изучали у детей от 1 до 16 лет в фармакокинетическом исследовании с однократным приемом препарата и в клиническом исследовании по изучению многократного приема препарата у небольшого числа детей в возрасте 3-12 лет. Скорость выведения активного метаболита с поправкой на массу тела у детей младшего возраста выше чем у взрослых, что приводит к более низким AUC по отношению к конкретной дозе. Прием препарата в дозе 2 мг/кг и однократных доз в 30 мг или 45 мг в соответствии с рекомендациями по дозированию для детей, приведенными в разделе "Способ применения и дозы", обеспечивает такую же AUC осельтамивира карбоксилата, какая достигается у взрослых после однократного приема капсулы с 75 мг препарата (что эквивалентно примерно 1 мг/кг). Фармакокинетика осельтамивира у детей старше 12 лет такая же, как у взрослых. Особые указания Нарушения психики У пациентов (в основном у детей и подростков), принимавших Тамифлю с целью лечения гриппа, были зарегистрированы нарушения со стороны психики, судороги и делирий- подобные психоневрологические нарушения. Эти случаи редко сопровождались опасными для жизни действиями. Роль Тамифлю в развитии этих явлений неизвестна. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших Тамифлю. Риск развития психоневрологических нарушений у пациентов, получающих Тамифлю, не превышает таковой у пациентов с гриппом, не получающих противовирусные препара- Рекомендуется тщательное наблюдение за состоянием и поведением пациентов, особенно детей и подростков, с целью выявления признаков анормального поведения и оценки риска продолжения приема препарата при развитии данных явлений. Данных по эффективности Тамифлю при любых заболеваниях, вызванных другими возбудителями, кроме вирусов гриппа А и В, нет. Препарат Тамифлю не является заменой вакцинации. Профилактический прием препарата Тамифлю возможен по эпидемиологическим показаниям. Рекомендации по коррекции дозы у больных с поражением ночек представлены в подразделе "Дозирование в особых случаях" (также см. "Фармакокинетика в особых группах пациентов"). Тамифлю в данной лекарственной форме не следует назначать детям младше 1 года. Инструкции по применению, обращению и уничтожению Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов. Влияние на способность управлять транспортными средствами: Исследования по изучению влияния препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из профиля безопасности, влияние Тамифлю на данные виды деятельности маловероятно. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25°С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Тамифлю® Международное непатентованное название:Осельтамивир. Форма выпуска:Капсулы. Состав: Одна капсула содержит: активное вещество: осельтамивир - 75 мг (в виде осельтамивира фосфата - 98.5 мг): вспомогательные вещества: крахмал прежелатинизированный - 46.4 мг, повидон К30 - 6.7 мг, кроскармеллоза натрия - 3.4 мг, тальк - 8.3 мг, натрия стеарилфумарат - 1.7 мг: оболочка капсулы - 63 мг (корпус - желатин, краситель железа оксид черный (Е172), титана диоксид (Е171): крышечка - желатин, краситель железа оксид красный (Е172), краситель железа оксид желтый (Е172), титана диоксид (Е171)): чернила для нанесения надписи на капсуле: этанол, шеллак, бутанол, титана диоксид (Е171), лак алюминиевый на основе индигокармина, этанол денатурированный [спирт метилированный]. АТХ: Регистрация: П N012090/01 Фармгруппа: Противовирусное средство. Дата регистрации: 09.06.2010. Окончание регстрации: . Описание:Твердые желатиновые капсулы, размер 2. Корпус - серый, непрозрачный: крышечка - светло-желтая, непрозрачная. Содержимое капсул - порошок от белого до желтовато- белого цвета. На капсуле имеется надпись "ROCHE" (на корпусе) и "75 mg" (на крышечке) светло-синего цвета. Примечание: по истечении 5 лет хранения препарата могут наблюдаться признаки "старения" капсул, что может привести к их повышенной хрупкости или другим нарушениям физического состояния, которые не оказывают влияния на эффективность и безопасность препарата. Упаковка:Капсулы 75 мг По 10 капсул в контурную ячейковую упаковку (блистер), изготовленную из триплекса (ПВХ/ПЭ/ПВДХ) и фольги алюминиевой. 1 блистер вместе с инструкцией по применению помещают в картонную пачку. Срок годности:7 лет. Не использовать но истечении срока годности, указанного на упаковке. Владелец рег.удостоверения:Хоффманн-Ля Рош Лтд. Производитель:F. Hoffmann-La Roche, Ltd. Представительство:Ф. Хоффманн-Ля Рош Лтд
894 Руб.Показания Лечение гриппа у взрослых и детей в возрасте старше 1 года. Профилактика гриппа у взрослых и подростков в возрасте старше 12 лет, находящихся в группах повышенного риска инфицирования вирусом (в воинских частях и больших производственных коллективах, у ослабленных больных). Профилактика гриппа у детей старше 1 года. Противопоказания Противопоказания Повышенная чувствительность к осельтамивиру или любому компоненту препарата. Терминальная стадия почечной недостаточности (клиренс креатинина <:10 мл/мин). Детский возраст до 1 года. Тяжелая печеночная недостаточность. С осторожностью: Беременность, период грудного вскармливания. Беременность Контролируемых исследований у беременных женщин не проводилось. Однако результаты постмаркетинговых и наблюдательных исследований продемонстрировали пользу предлагаемого стандартного режима дозирования для данной популяции пациентов. Результаты фармакокинетического анализа показали более низкую экспозицию активного метаболита (приблизительно на 30% в течение всех триместров беременности) у беременных женщин по сравнению с не беременными. Тем не менее, значение расчетной экспозиции остается выше ингибирующих концентраций (значение IC95) и терапевтических значений для многих штаммов вируса гриппа. Изменение режима дозирования у беременных женщин при проведении терапии или профилактики не рекомендуется (см. раздел "Фармакокинетика в особых группах пациентов"). Не обнаружено прямого или опосредованного неблагоприятного влияния препарата на беременность, эмбрио-фетальное или постна- тальное развитие (см. "Доклинические данные"). При назначении Тамифлю® беременным женщинам следует учитывать как данные по безопасности, так и течение беременности и патогенность циркулирующего штамма вируса гриппа. Во время доклинических исследований осельтамивир и активный метаболит проникали в молоко лактирующих крыс. Данные по экскреции осельтамивира с грудным молоком у человека и применению осельтамивира кормящими женщинами ограничены. Осельтами- вир и его активный метаболит в небольших количествах проникают в грудное молоко (см. "Доклинические данные"), создавая субтерапевтические концентрации в крови грудного ребенка. При назначении осельтамивира кормящим женщинам следует также учитывать сопутствующее заболевание и патогенность циркулирующего штамма вируса гриппа. При беременности и в период [рудного вскармливания осельтамивир применяют только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода и ребенка. Применение и дозы Внутрь, во время еды или независимо от приема пищи. Переносимость препарата можно улучшить, если принимать его во время еды. Взрослые, подростки или дети, которые не могут проглотить капсулу, также могут получать лечение Тамифлю в лекарственной форме "порошок для приготовления суспензии для приема внутрь". В случаях, когда Тамифлю® в лекарственной форме "порошок для приготовления суспензии для приема внутрь" отсутствует, или при наличии признаков "старения" капсул (например, повышенная хрупкость или другие нарушения физического состояния), необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 чайная ложка) подходящего подслащенного продукта питания (шоколадный сироп с нормальным содержанием сахара или без содержания сахара, мед, светло-коричневый сахар или столовый сахар, растворенный в воде, сладкий десерт, сгущенное молоко с сахаром, яблочное пюре или йогурт) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же по- еле приготовления. Подробные рекомендации даны в подразделе "Экстемпоральное приготовление суспензии Тамифлю". Стандартный режим дозирования Лечение Прием препарата необходимо начинать не позднее 2 суток с момента развития симптомов заболевания. Взрослые и подростки в возрасте >:12 лет По 75 мг 2 раза в сутки внутрь в течение 5 дней. Увеличение дозы более 150 мг/сутки не приводит к усилению эффекта. Дети с массой тела >:40 кг или в возрасте от 8 до 12 лет Дети, которые умеют проглатывать капсулы, также могут получать лечение, принимая по одной капсуле 75 мг 2 раза в сутки в течение 5 дней. Дети в возрасте от 1 года до 8 лет Рекомендуется Тамифлю порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг (для детей старше 2 лет). Для определения рекомендованного режима дозирования смотрите инструкции по медицинскому применению Тамифлю порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг. Возможно экстемпоральное приготовление суспензии с использованием капсул 75 мг (см. подраздел "Экстемпоральное приготовление суспензии Тамифлю"). Профилактика Прием препарата необходимо начинать не позднее 2 суток после контакта с больными. Взрослые и подростки в возрасте >:12 лет По 75 мг 1 раз в сутки внутрь в течение не менее 10 дней после контакта с больным. Во время сезонной эпидемии гриппа - по 75 мг 1 раз в сутки в течение 6 недель. Профилактическое действие продолжается столько, сколько длится прием препарата. Дети с массой тела >:40 кг или в возрасте от 8 до 12 лет Дети, которые могут проглатывать капсулы, также могут получать профилактическую терапию, принимая по одной капсуле 75 мг 1 раз в сутки в течение 10 дней. Дети в возрасте от 1 года до 8 лет Рекомендуется Тамифлю порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг. Для определения рекомендованного режима дозирования смотрите инструкции по медицинскому применению Тамифлю® порошок для приготовления суспензии для приема внутрь 12 мг/мл или капсулы 30 и 45 мг. Возможно экстем- поральное приготовление суспензии с использованием капсул 75 мг (см. раздел "Экстемпоральное приготовление суспензии Тамифлю"). Дозирование в особых случаях Больные с поражением почек Лечение Больным с клиренсом креатинина более 60 мл/мин коррекции дозы не требуется. У боль- ных с клиренсом креатинина от 30 до 60 мл/мин дозу Тамифлю следует уменьшить до 30 мг два раза в сутки в течение 5 дней. У больных с клиренсом креатинина от 10 до 30 мл/мин дозу Тамифлю следует уменьшить до 30 мг один раз в сутки в течение 5 дней. Пациентам, находящимся на постоянном гемодиализе, Тамифлю в первоначальной дозе 30 мг можно принять до начала диализа, если симптомы гриппа появились в течение 48 ч между сеансами диализа. Для поддержания плазменной концентрации на терапевтическом уровне Тамифлю следует принимать по 30 мг после каждого сеанса диализа. Пациентам, находящимся на перитонеальном диализе, Тамифлю следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем но 30 мг каждые 5 дней (см. также "Дозирование в особых случаях" и "Особые указания"). Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина <:10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют. Профилактика Больным с клиренсом креатинина более 60 мл/мин коррекции дозы не требуется. У боль- ных с клиренсом креатинина от 30 до 60 мл/мин дозу Тамифлю следует уменьшить до 30 мг один раз в сутки. У больных с клиренсом креатинина от 10 до 30 мл/мин рекомендуется уменьшить дозу Тамифлю до 30 мг через день. Пациентам, находящимся на постоянном гемодиализе, Тамифлю в первоначальной дозе 30 мг можно принять до начала диализа ("1-й сеанс"). Для поддержания плазменной концентрации на терапевтическом уровне Тамифлю следует принимать по 30 мг после каждого последующего нечетного сеанса диализа. Пациентам, находящимся на перитонеальном диализе, Тамифлю следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем по 30 мг каждые 7 дней (см. также "Дозирование в особых случаях" и "Особые указания"). Фармакокинетика осельтами- вира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креа- тинина <:10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсу тствуют. Больные с поражением печени Коррекции дозы при лечении и профилактике гриппа у пациентов с нарушением функции печени легкой и средней степени тяжести не требуется. Безопасность и фармакокинетика Тамифлю у пациентов с тяжелыми нарушениями функции печени не изучалась. Больные пожилого и старческого возраста Коррекции дозы для профилактики или лечения гриппа не требуется. Вольные с ослабленным иммунитетом (после трансплантации) Для сезонной профилактики гриппа у больных с ослабленным иммунитетом в возрасте >:1 года - в течение 12 недель, коррекции дозы не требуется (см. раздел "Способ применения и дозы"). Дети Тамифлю® в данной лекарственной форме не следует назначать детям до 1 года. Экстемпоральное приготовление суспензии Тамифлю В случаях, когда у взрослых, подростков и детей существует проблема с проглатыванием капсул, а Тамифлю в лекарственной форме "порошок для приготовления суспензии для приема внутрь" отсутствует или при наличии признаков "старения" капсул, необходимо открыть капсулу и высыпать ее содержимое в небольшое количество (максимально 1 чайная ложка) подходящего подслащенного продукта питания (см. выше) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же после приготовления. Если пациентам требуется доза 75 мг то необходимо следовать следующим инструкциям: 1. Держа одну капсулу 75 мг Тамифлю над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость. 2. Добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания (чтобы скрыть горький вкус) и хорошо перемешать. 3. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь. Если пациентам требуются дозы 30-60 мг, то для правильного дозирования необходимо следовать следующим инструкциям: 1. Держа одну капсулу 75 мг Тамифлю над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость. 2. Добавить в порошок 5 мл воды с помощью шприца с метками, показывающими количество набранной жидкости. Тщательно перемешать в течение 2 минут. 3. Набрать в ширин необходимое количество смеси из емкости согласно нижеприве ТАБЛИЦЪ Нет необходимости в заборе нерастворенного белого порошка, поскольку он является неактивным наполнителем. Нажав на поршень шприца, ввести все его содержимое во вторую емкость. Оставшуюся неиспользованную смесь необходимо выбросить. 4. Во вторую емкость добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания, чтобы скрыть горький вкус, и хорошо перемешать. 5. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь. Повторяйте данную процедуру перед каждым приемом препарата. Побочные эффекты и передозировка Побочные эффекты: В исследованиях по лечению гриппа у взрослых/пациентов подросткового возраста самыми частыми нежелательными реакциями (HP) были тошнота, рвота и головная боль. Большинство IIP возникали в первый или второй день лечения и проходили самостоятельно в течение 1-2 дней. В исследованиях по профилактике гриппа у взрослых и подростков самыми частыми НP были тошнота, рвота, головная боль и боль. У детей наиболее часто встречалась рвота. Описанные HP в большинстве случаев не требовали отмены препарата. Лечение и профилактика гриппа у взрослых и подростков В таблице 1 представлены НP, возникавшие наиболее часто (>:1%) при приеме рекомендованной дозы Тамифлю в исследованиях по профилактике и лечению гриппа у взрослых и подростков (75 мг 2 раза в сутки в течение 5 дней для лечения и 75 мг 1 раз в сутки до 6 недель для профилактики), и частота которых как минимум на 1% выше по сравнению с плацебо. В исследования по лечению гриппа вошли взрослые/подростки без сопутствующей патологии и больные группы риска, т.е. пациенты с высоким риском развития осложнений гриппа (пациенты пожилого и старческого возраста, пациенты с хроническими заболеваниями сердца или органов дыхания). В целом профиль безопасности у пациентов группы риска соответствовал таковому у взрослых/пациентов подросткового возраста без сопутствующей патологии. В исследованиях по профилактике гриппа профиль безопасности у пациентов, получав- ших рекомендованную дозу Тамифлю (75 мг 1 раз в сутки до 6 недель), не отличался от такового в исследованиях по лечению гриппа, несмотря на более длительный прием препарата. лечение - дерматит (включая аллергический и атопический дерматит, 1% против 2%). Нарушения со стороны органа слуха и лабиринтные нарушения (Тамифлю против плацебо): лечение - боль в ухе (1% против 1%). Нарушения со стороны органа зрения (Тамифлю против плацебо): лечение- конъюнктивит (включая покраснение глаз, выделения из глаза и боль в глазах, 1% против <:1%). Дополнительные нежелательные явления, отмеченные при проведении лечения гриппа у детей, не соответствовавшие описанным выше критериям. Нарушения со стороны крови и лимфатической системы (Тамифлю против плацебо): лечение - лимфоаденопатия (<:1% против 1%). Нарушения со стороны органа слуха и лабиринтные нарушения (Тамифлю против плацебо): лечение - повреждение барабанной перепонки (<:1% против 1%). Постмаркетинговое наблюдение Далее представлены нежелательные явления при применении Тамифлю, которые наблюдались в период постмаркетингового наблюдения. Частота данных нежелательных явлений и/или причинно-следственная связь с применением препарата Тамифлю® не может быть установлена, так как не известен истинный размер популяции в виду добровольного характера сообщений. Нарушения со стороны кожи и подкожных тканей: реакции гиперчувствительности - дерматит, кожная сыпь, экзема, крапивница, мультиформная экссудативная эритема, синдром Стивенса-Джонсона и токсический эпидермальный некролиз, аллергия, анафилактические и анафилактоидные реакции, отек Квинке. Нарушения со стороны печени и желчевыводящих путей: гепатит, увеличение активности "печеночных" ферментов у пациентов с гриппоподобными симптомами, получавших Тамифлю: фульминантный гепатит (в том числе с фатальным исходом), печеночная недостаточность, желтуха. Нарушения со стороны нервно-психической сферы Гриппозная инфекция может ассоциироваться с различными неврологическими симптомами и изменениями поведения, включая такие симптомы, как галлюцинации, бред и анормальное поведение. В некоторых случаях они могут привести к смертельному исходу. Такие явления могут возникать как на фоне развития энцефалопатии или энцефалита, так и без проявления данных заболеваний. У пациентов (в основном у детей и подростков), принимавших Тамифлю с целью лечения гриппа, были зарегистрированы судороги и делирий (включая такие симптомы, как нарушение сознания, дезориентация во времени и пространстве, анормальное поведение, бред, галлюцинации, возбуждение, тревога, ночные кошмары). Эти случаи редко сопро- вождались опасными для жизни действиями. Роль Тамифлю в развитии этих явлений неизвестна. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших Тамифлю. Нарушения со стороны желудочно-кишечного тракта: желудочно-кишечные кровотечения после приема Тамифлю® (в частности, нельзя исключить связь между явлениями геморрагического колита и приемом Тамифлю, поскольку указанные явления исчезали как после выздоровления пациента от гриппа, так и после отмены препарата). Нарушения со стороны органа зрения: нарушение зрения. Нарушения со стороны сердца: аритмия. Передозировка: В большинстве случаев передозировка в ходе клинических исследований и при постмар- кетинговом применении Тамифлю не сопровождалась какими-либо нежелательными явлениями. В остальных случаях симптомы передозировки соответствовали нежелательным явлениям, представленным в разделе "Побочное действие". Взаимодействие с другими ЛС: Клинически значимые лекарственные взаимодействия маловероятны по данным фармакологических и фармакокинетических исследований. Осельтамивир экстенсивно превращается в активный метаболит под действием эстераз, в основном расположенных в печени. Лекарственные взаимодействия, обусловленные конкуренцией за связывание с активными центрами эстераз, в литературных источниках широко не представлены. Низкая степень связывания осельтамивира и активного метаболита с белками плазмы не дают оснований предполагать наличие взаимодействий, связанных с вытеснением лекарственных средств из связи с белками. Исследования in vitro показывают, что ни осельтамивир, ни его активный метаболит не являются предпочтительным субстратом для полифункциональных оксидаз системы цитохрома Р450 или для глюкуронилтрансфераз (см. подраздел "Фармакокинетика"). Оснований для взаимодействия с пероральными контрацептивами нет. Циметидин, неспецифический ингибитор изоферментов системы цитохрома Р450 и конкурирующий в процессе канальцевой секреции с препаратами щелочного типа и катионами, не влияет на плазменные концентрации осельтамивира и его активного метаболита. Маловероятны клинически значимые межлекарственные взаимодействия, связанные с конкуренцией за канальцевую секрецию, принимая во внимание резерв безопасности для большинства подобных препаратов, пути выведения активного метаболита осельтамивира (клубочковая фильтрация и анионная канальцевая секреция), а также выводящую способность каждого из путей. Пробенецид приводит к увеличению AUC активного метаболита осельтамивира примерно в 2 раза (за счет снижения активной канальцевой секреции в почках). Однако коррекции дозы при одновременном применении с пробенецидом не требуется, учитывая резерв безопасности активного метаболита. Одновременный прием с амоксициллином не влияет на плазменные концентрации осель- тамивира и его компонентов, демонстрируя слабую конкуренцию за выведение путем анионной канальцевой секреции. Одновременный прием с парацетамолом не влияет на плазменные концентрации осельтамивира и его активного метаболита или парацетамола. Фармакокинетических взаимодействий между осельтамивиром, его основным метаболитом не обнаружено при одновременном приеме с парацетамолом, ацетилсалициловой кислотой, циметидином, антацидными средствами (магния и алюминия гидроксид, кальция карбонат), варфарином, римантадином или амантадином. При использовании Тамифлю с часто применяемыми препаратами, такими как ингибиторы АПФ (эналаприл, каптоприл), тиазидные диуретики (бендрофлуметиазид), антибиотики (пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин), блокато- ры Н2-гистаминовых рецепторов (ранитидин, циметидин), бета-адреноблокаторы (про- пранолол), ксантины (теофиллин), симпатомиметики (псевдоэфедрин), опиаты (кодеин), глюкокортикостероиды, ингаляционные бронхолитики и ненаркотические анальгетики (ацетилсалициловая кислота, ибупрофен и парацетамол), изменений характера или частоты нежелательных явлений не наблюдалось. Применять осельтамивир в комбинации с препаратами, имеющими узкую широту терапевтического действия (например, хлорпропамид, метотрексат, бутадион), необходимо с осторожностью. Фармакологическое действие и фармакокинетика Механизм действия Противовирусный препарат. Осельтамивир является пролекарством, его активный метаболит (осельтамивира карбоксилат, ОК) - эффективный и селективный ингибитор нейра- минидазы вирусов гриппа типа А и В - фермента, катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновения в неинфицированные клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме. Тормозит рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo, уменьшает выделение вирусов гриппа А и В из организма. Концентрация ОК, необходимая для ингибирования нейраминидазы на 50% (IC50), составляет 0.1-1.3 нМ для вируса гриппа А и 2.6 нМ для вируса гриппа В. Медиана значений IC50 для вируса гриппа В несколько выше и составляет 8.5 нМ. Клиническая эффективность В проведенных исследованиях Тамифлю не оказывал влияния на образование противогриппозных антител, в том числе на выработку антител в ответ на введение инактивированной вакцины против гриппа. Исследования естественной гриппозной инфекции В клинических исследованиях, проведенных во время сезонной инфекции гриппа, пациенты начинали получать Тамифлю® не позднее 40 ч после появления первых симптомов гриппозной инфекции. 97% пациентов были инфицированы вирусом гриппа А и 3% пациентов - вирусом гриппа В. Тамифлю значительно сокращал период клинических проявлений гриппозной инфекции (на 32 ч). У пациентов с подтвержденным диагнозом гриппа, принимавших Тамифлю, тяжесть заболевания, выраженная как площадь под кривой для суммарного индекса симптомов, была на 38% меньше по сравнению с пациентами, получавшими плацебо. Болес того, у молодых пациентов без сопутствующих заболеваний Та- мифлю снижал примерно на 50% частоту развития осложнений гриппа, требующих применения антибиотиков (бронхита, пневмонии, синусита, среднего отита). Были получены четкие доказательства эффективности препарата в отношении вторичных критериев эффективности, относящихся к антивирусной активности: Тамифлю вызывал как укорочение времени выделения вируса из организма, так и уменьшение площади под кривой "вирусные тигры-время". Данные, полученные в исследовании по терапии Тамифлю у больных пожилого и старческого возраста, показывают, что прием Тамифлю в дозе 75 мг 2 раза в сутки в течение 5 дней сопровождался клинически значимым уменьшением медианы периода клинических проявлений гриппозной инфекции, аналогичным таковому у взрослых пациентов более молодого возраста, однако различия не достигли статистической значимости. В другом исследовании больные гриппом старше 13 лет, имевшие сопутствующие хронические заболевания сердечно-сосудистой и/или дыхательной систем, получали Тамифлю в том же режиме дозирования или плацебо. Отличий в медиане периода до уменьшения клинических проявлений гриппозной инфекции в группах Тамифлю и плацебо не было, однако период повышения температуры при приеме Тамифлю сокращался примерно на 1 день. Доля пациентов, выделяющих вирус на 2-ой и 4-ый день, становилась значительно меньше. Профиль безопасности Тамифлю у пациентов группы риска не отличался от такового в общей популяции взрослых пациентов. Лечение гриппа у детей У детей в возрасте 1-12 лет (средний возраст 5.3 года), имевших лихорадку (>:37.8оС) и один из симптомов со стороны дыхательной системы (кашель или ринит) в период циркуляции вируса гриппа среди населения, было проведено двойное слепое плацебо- контролируемое исследование. 67% пациентов были инфицированы вирусом гриппа А и 33% пациентов - вирусом гриппа В. Препарат Тамифлю (при приеме не позднее 48 ч после появления первых симптомов гриппозной инфекции) значительно снижал продолжительность заболевания (на 35.8 ч) по сравнению с плацебо. Продолжительность заболевания определялась как время до купирования кашля, заложенности носа, исчезновения лихорадки, возвращения к обычной активности. В группе детей, получавших Тамифлю®, частота острого среднего отита снижалась на 40% по сравнению с группой плацебо. Выздоровление и возвращение к обычной активности наступало почти на 2 дня раньше у детей, получавших Тамифлю®, по сравнению с группой плацебо. В другом исследовании участвовали дети в возрасте 6-12 лет, страдающие бронхиальной астмой: 53.6% пациентов имели гриппозную инфекцию, подтвержденную серологически и/или в культуре. Медиана продолжительности заболевания в группе пациентов, полу- чавших Тамифлю , значительно не снижалась. Но к последнему 6-му дню терапии Тамифлю® объем форсированного выдоха за 1 сек (ОФВ1) повышался на 10.8% по сравнению с 4.7% у пациентов, получавших плацебо (р=0.0148). Профилактика гриппа у взрослых и подростков Профилактическая эффективность Тамифлю при естественной гриппозной инфекции А и В была доказана в 3 отдельных клинических исследованиях III фазы. На фоне приема Тамифлю® гриппом заболели около 1% пациентов. Тамифлю® также значительно уменьшал частоту выделения вируса и предотвращал передачу вируса от одного члена семьи к другому. Взрослые и подростки, которые были в контакте с больным членом семьи, начинали прием Тамифлю® в течение двух дней после возникновения симптомов гриппа у членов семьи и продолжали его в течение 7 дней, что достоверно уменьшало частоту случаев гриппа у контактировавших лиц на 92%. У непривитых и в целом здоровых взрослых в возрасте 18-65 лет прием Тамифлю во время эпидемии гриппа существенно снижал заболеваемость гриппом (на 76%). Пациенты принимали препарат в течение 42 дней. У лиц пожилого и старческого возраста, находившихся в домах для престарелых, 80% из которых были привиты перед сезоном, когда проводилось исследование, Тамифлю достоверно снижал заболеваемость гриппом на 92%. В том же исследовании Тамифлю достоверно (на 86%) уменьшал частоту осложнений гриппа: бронхита, пневмонии, синусита. Пациенты принимали препарат в течение 42 дней. Профилактика гриппа у детей Профилактическая эффективность Тамифлю при естественной гриппозной инфекции была продемонстрирована у детей от 1 года до 12 лет после контакта с заболевшим членом семьи или с кем-то из постоянного окружения. Основным параметром эффективности была частота лабораторно подтвержденной гриппозной инфекции. У детей, получавших Тамифлю /порошок для приготовления суспензии для приема внутрь/ в дозе от 30 до 75 мг 1 раз в день в течение 10 дней и не выделявших вирус исходно, частота лабораторно подтвержденного гриппа уменьшилась до 4% (2/47) по сравнению с 21% (15/70) в группе плацебо. Профилактика гриппа у лиц с ослабленным иммунитетом У лиц с ослабленным иммунитетом при сезонной гриппозной инфекции и при отсутствии вирусовыделения исходно, профилактическое применение Тамифлю приводило к снижению частоты лабораторно подтвержденной гриппозной инфекции, сопровождающейся клинической симптоматикой, до 0.4% (1/232) по сравнению с 3% (7/231) в группе плацебо. Лабораторно подтвержденная гриппозная инфекция, сопровождающаяся клинической симптоматикой, диагностировалась при наличии температуры в полости рта выше 37.2°С, кашля и/или острого ринита (все зарегистрированные в один и тот же день во время приема препарата/плацебо), а также положительного результата обратно-транскриптазной полимеразной цепной реакции на РНК вируса гриппа. Резистентность Клинические исследования Риск появления вирусов гриппа со сниженной чувствительностью или резистентностью к препарату изучался в клинических исследованиях, спонсированных компанией Рош. У всех пациентов-носителей OK-резистентного вируса носительство имело временный характер, не влияло па элиминацию вируса и не вызывало ухудшения клинического состояния. ТАБЛИЦЪ При приеме Тамифлю с целью постконтактной профилактики (7 дней), профилактики контактировавших в семье (10 дней) и сезонной профилактики (42 дня) у лиц с нормальной функцией иммунной системы случаев резистентности к препарату не отмечено. В 12-недельном исследовании по сезонной профилактике у лиц с ослабленным иммунитетом случаев возникновения резистентности также не наблюдалось. Данные отдельных клинических случаев и наблюдательных исследовании У пациентов, не получавших осельтамивир, обнаружены возникающие в природных условиях мутации вирусов гриппа А и В, которые обладали сниженной чувствительностью к осельтамивиру. В 2008 году мутация по типу замены H275Y. приводящая к резистентности, была обнаружена более чем у 99% штаммов вируса 2008 Н1N1, циркулирующих в Европе. Вирус гриппа 2009 H1N1 ("свиной грипп") в большинстве случаев был чувствителен к осельтамивиру. Устойчивые к осельтамивиру штаммы обнаружены у лиц с нормальной функцией иммунной системы и лиц с ослабленным иммунитетом, принимавших осельта- мивир. Степень снижения чувствительности к осельтамивиру и частота встречаемости подобных вирусов может отличаться в зависимости от сезона и региона. Устойчивость к осельтамивиру обнаружена у пациентов с пандемическим гриппом H1N1, получавших препарат как для лечения, так и для профилактики. Частота встречаемости резистентности может быть выше у более молодых пациентов и пациентов с ослабленным иммунитетом. Устойчивые к осельтамивиру лабораторные штаммы вирусов гриппа и вирусы гриппа от пациентов, получавших терапию осельтами- виром, несут мутации нейраминидазы N1 и N2. Мутации, приводящие к устойчивости, часто являются специфическими для подтипа нейраминидазы. При принятии решения о применении Тамифлю следует учитывать сезонную чувствительность вируса гриппа к препарату (последнюю информацию можно найти на сайте ВОЗ). Доклинические данные Доклинические данные, полученные на основании стандартных исследований по изучению фармакологической безопасности, генотоксичности и хронической токсичности, не выявили особой опасности для человека. Канцерогенность: результаты 3-х исследований по выявлению канцерогенного потенциала (двух 2-х летних исследований на крысах и мышах для осельтамивира и одного 6-ти месячного исследования на трансгенных мышах Tg:AC для активного метаболита) были отрицательными. Мутагенность: стандартные генотоксические тесты для осельтамивира и активного метаболита были отрицательными. Влияние на фертильность: осельтамивир в дозе 1500 мг/кг/сут не влиял на генеративную функцию самцов и самок крыс. Тератогенность: в исследованиях по изучению тератогенности осельтамивира в дозе до 1500 мг/кг/сут (на крысах) и до 500 мг/кг/сут (на кроликах) влияния на эмбрио-фетальное развитие не обнаружено. В исследованиях но изучению антенатального и постнатального периодов развития у крыс при введении осельтамивира в дозе 1500 мг/кг/сут наблюдалось увеличение периода родов: предел безопасности между экспозицией для человека и максимальной не оказывающей эффекта дозой у крыс (500 мг/кг/сут) для осельтамивира выше в 480 раз, а для его активного метаболита - в 44 раза. Экспозиция у плода составляла 15- 20% от таковой у матери. Прочее: осельтамивир и активный метаболит проникают в молоко лактирующих крыс. Согласно ограниченным данным осельтамивир и его активный метаболит проникают в грудное молоко человека. По результатам экстраполяции данных, полученных в исследованиях у животных, их количество в грудном молоке может составлять 0.01 мг/сутки и 0.3 м г/сутки, соответственно. Примерно у 50% протестированных морских свинок при введении максимальных доз активной субстанции осельтамивира наблюдалась сенсибилизация кожи в виде эритемы. Также выявлено обратимое раздражение глаз у кроликов. В то время как очень высокие пероральные однократные дозы (657 мг/кг и выше) осельтамивира не оказывали влияния на взрослых крыс, данные дозы оказывали токсическое действие на незрелых 7-дневных детенышей крыс, в том числе приводили к гибели животных. Нежелательных эффектов не наблюдалось при хроническом введении в дозе 500 мг/кг/сут с 7 по 21 день постнаталыюго периода. Фармакокинетика: Всасывание Осельтамивир легко всасывается в желудочно-кишечном тракте и экстенсивно превращается в активный метаболит под действием печеночных и кишечных эстераз. Концентрации активного метаболита в плазме определяются в пределах 30 мин, время достижения максимальной концентрации 2-3 ч, и более чем в 20 раз превышают концентрации пролекарства. Не менее 75% принятой внутрь дозы попадает в системный кровоток в виде активного метаболита, менее 5% - в виде исходного препарата. Плазменные концентрации как пролекарства, так и активного метаболита пропорциональны дозе и не зависят от приема пищи. Распределение Объем распределения (Vss) активного метаболита - 23 л. По данным исследований, проведенных на животных, после приема внутрь осельтамивира его активный метаболит обнаруживался во всех основных очагах инфекции (легких, промывных водах бронхов, слизистой оболочке полости носа, среднем ухе и трахее) в концентрациях, обеспечивающих противовирусный эффект. Связь активного метаболита с белками плазмы - 3%. Связь пролекарства с белками плазмы - 42%, что недостаточно, чтобы служить причиной существенных лекарственных взаимодействий. Метаболизм Осельтамивир экстенсивно превращается в активный метаболит под действием эстераз, находящихся преимущественно в печени. Ни осельтамивир, ни активный метаболит не являются субстратами или ингибиторами изоферментов системы цитохрома Р450. Выведение Выводится (>:90%) в виде активного метаболита преимущественно почками. Активный метаболит не подвергается дальнейшей трансформации и выводится почками (>:99%) путем клубочковой фильтрации и канальцевой секреции. Почечный клиренс (18.8 л/ч) превышает скорость клубочковой фильтрации (7.5 л/ч), что указывает на то, что препарат выводится еще и путем канальцевой секреции. Через кишечник выводится менее 20% принятого препарата. Период полувыведения активного метаболита 6-10 ч. Фармакокинетика в особых группах пациентов Больные с поражением почек При применении Тамифлю (100 мг два раза в сутки в течение 5 дней) у больных с различной степенью поражения почек площадь под кривой "концентрация активного метаболита в плазме - время" (AUC оселыамнвира карбоксилата) обратно пропорциональна снижению функции почек. Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина <:10 мл/мин), не находящихся на диализе, не изучалась. Больные с поражением печени Полученные in vitro и в исследованиях на животных данные об отсутствии значительного повышения AUC осельтамивира или его активного метаболита при нарушении функции печени легкой и средней степени тяжести были подтверждены и в клинических исследованиях (см. "Дозирование в особых случаях"). Безопасность и фармакокинетика оссльта- мивира у пациентов с тяжелым нарушением функции печени не изучалась. Вольные пожилого и старческого возраста У больных пожилого и старческого возраста (65-78 лет) экспозиция активного метаболита в равновесном состоянии на 25-35% выше, чем у более молодых пациентов при назначении аналогичных доз Тамифлю. Период полувыведения препарата у больных пожилого и старческого возраста существенно не отличался от такового у более молодых пациентов. С учетом данных по экспозиции препарата и его переносимости больными пожилого и старческого возраста коррекции дозы при лечении и профилактике гриппа не требуется. Лети в возрасте от 1 года до 8 лет и подростки Фармакокинетику Тамифлю изучали у детей от 1 до 16 лет в фармакокинетическом исследовании с однократным приемом препарата и в клиническом исследовании по изучению многократного приема препарата у небольшого числа детей в возрасте 3-12 лет. Скорость выведения активного метаболита с поправкой на массу тела у детей младшего возраста выше чем у взрослых, что приводит к более низким AUC по отношению к конкретной дозе. Прием препарата в дозе 2 мг/кг и однократных доз в 30 мг или 45 мг в соответствии с рекомендациями по дозированию для детей, приведенными в разделе "Способ применения и дозы", обеспечивает такую же AUC осельтамивира карбоксилата, какая достигается у взрослых после однократного приема капсулы с 75 мг препарата (что эквивалентно примерно 1 мг/кг). Фармакокинетика осельтамивира у детей старше 12 лет такая же, как у взрослых. Особые указания Нарушения психики У пациентов (в основном у детей и подростков), принимавших Тамифлю с целью лечения гриппа, были зарегистрированы нарушения со стороны психики, судороги и делирий- подобные психоневрологические нарушения. Эти случаи редко сопровождались опасными для жизни действиями. Роль Тамифлю в развитии этих явлений неизвестна. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших Тамифлю. Риск развития психоневрологических нарушений у пациентов, получающих Тамифлю, не превышает таковой у пациентов с гриппом, не получающих противовирусные препара- Рекомендуется тщательное наблюдение за состоянием и поведением пациентов, особенно детей и подростков, с целью выявления признаков анормального поведения и оценки риска продолжения приема препарата при развитии данных явлений. Данных по эффективности Тамифлю при любых заболеваниях, вызванных другими возбудителями, кроме вирусов гриппа А и В, нет. Препарат Тамифлю не является заменой вакцинации. Профилактический прием препарата Тамифлю возможен по эпидемиологическим показаниям. Рекомендации по коррекции дозы у больных с поражением ночек представлены в подразделе "Дозирование в особых случаях" (также см. "Фармакокинетика в особых группах пациентов"). Тамифлю в данной лекарственной форме не следует назначать детям младше 1 года. Инструкции по применению, обращению и уничтожению Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов. Влияние на способность управлять транспортными средствами: Исследования по изучению влияния препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из профиля безопасности, влияние Тамифлю на данные виды деятельности маловероятно. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25°С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Тамифлю® Международное непатентованное название:Осельтамивир. Форма выпуска:Капсулы. Состав: Одна капсула содержит: активное вещество: осельтамивир - 75 мг (в виде осельтамивира фосфата - 98.5 мг): вспомогательные вещества: крахмал прежелатинизированный - 46.4 мг, повидон К30 - 6.7 мг, кроскармеллоза натрия - 3.4 мг, тальк - 8.3 мг, натрия стеарилфумарат - 1.7 мг: оболочка капсулы - 63 мг (корпус - желатин, краситель железа оксид черный (Е172), титана диоксид (Е171): крышечка - желатин, краситель железа оксид красный (Е172), краситель железа оксид желтый (Е172), титана диоксид (Е171)): чернила для нанесения надписи на капсуле: этанол, шеллак, бутанол, титана диоксид (Е171), лак алюминиевый на основе индигокармина, этанол денатурированный [спирт метилированный]. АТХ: Регистрация: П N012090/01 Фармгруппа: Противовирусное средство. Дата регистрации: 09.06.2010. Окончание регстрации: . Описание:Твердые желатиновые капсулы, размер 2. Корпус - серый, непрозрачный: крышечка - светло-желтая, непрозрачная. Содержимое капсул - порошок от белого до желтовато- белого цвета. На капсуле имеется надпись "ROCHE" (на корпусе) и "75 mg" (на крышечке) светло-синего цвета. Примечание: по истечении 5 лет хранения препарата могут наблюдаться признаки "старения" капсул, что может привести к их повышенной хрупкости или другим нарушениям физического состояния, которые не оказывают влияния на эффективность и безопасность препарата. Упаковка:Капсулы 75 мг По 10 капсул в контурную ячейковую упаковку (блистер), изготовленную из триплекса (ПВХ/ПЭ/ПВДХ) и фольги алюминиевой. 1 блистер вместе с инструкцией по применению помещают в картонную пачку. Срок годности:7 лет. Не использовать но истечении срока годности, указанного на упаковке. Владелец рег.удостоверения:Хоффманн-Ля Рош Лтд. Производитель:F. Hoffmann-La Roche, Ltd. Представительство:Ф. Хоффманн-Ля Рош Лтд

